RESEARCH
おたまじゃくしの尾が消えるしくみ
尾を非自己と見なすカエルの免疫系
おたまじゃくしがカエルになる時、ほとんどの器官は幼生型から成体型へ大規模につくり換えられ、外来の異物から体を守る免疫系も細胞が入れ換わり自己・非自己の認識が厳しくなります。皮膚も成体型へ変化しますが、やがて消える尾の皮膚だけは幼生型のままです。井筒ゆみさんはこの現象に注目し、これまで甲状腺ホルモンのはたらきを中心に研究されてきた尾の消失について「成体の免疫細胞に拒絶されて消える」という仮説をたてました。体づくりのしくみに新たな概念を投げかける研究です。
1.おたまじゃくしからカエルへの劇的な変化
ひれを持ち尾をくねらせ泳いでいたおたまじゃくしに足が生えカエルになる時、その体の中でどのような変化が起きているのだろう。おたまじゃくしからカエルへの変態期には、さまざまな器官で幼生(おたまじゃくし)型から成体(カエル)型への大規模なつくり換えが起き心臓や腸なども変化する。特に、体の体積の約半分をしめていた尾ではすべての組織で細胞死が起き、ひれが消失し徐々に短くなった尾は最終的に消える(図1)。これまでこのしくみは、甲状腺ホルモンが血中で増えることをきっかけに細胞が自ら死ぬのだと説明されてきた。
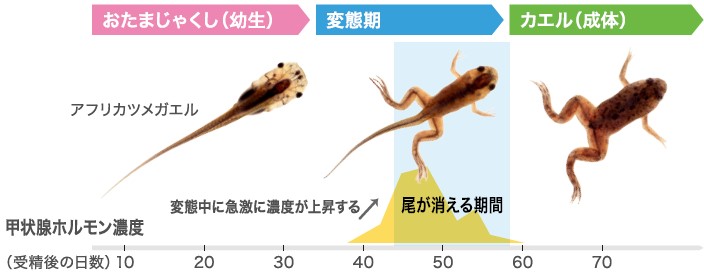
(図1)カエルの変態
変態期には免疫系の機能も幼生型から成体型へと変わる(図2)。多くの脊椎動物と同じくカエルの成体は他の個体、正確にはMHC(註1)が異なった個体の皮膚を拒絶する。一方、幼生の免疫系はMHCが完全に異なる系統の皮膚は拒絶するが、異系統と同系統をかけ合わせた半分自分とMHCが異なる個体の皮膚は拒絶しない。つまり、幼生型免疫細胞は比較的寛容なのである。
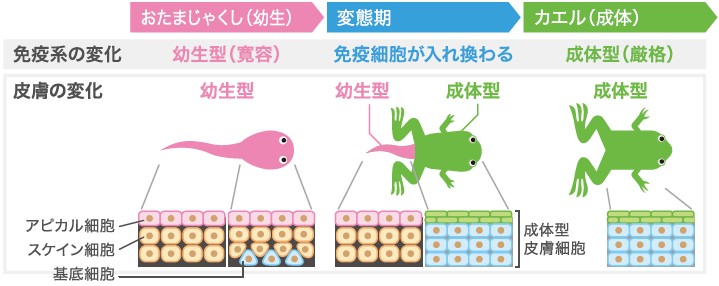
(図2)免疫系と皮膚の変化
皮膚にも明瞭な変化が起こる。幼生の皮膚は魚などの水棲動物に特有の細胞として知られるスケイン細胞と、最外層に存在し細胞同士がすき間なく密着していることで体を保護しているアピカル細胞の2種類で構成されている。成体になるとスケイン細胞もアピカル細胞も消え、変態期につくられる基底細胞から成体型の皮膚が形成され、最外層が角質化し、毛こそ生えないが哺乳類の皮膚と基本的に同じ構造になる。しかし、この変化には大きな特徴がある。それは部域特異性があることだ。成体型への変化は胴体だけで起こり、尾では起こらない。皮膚は全身を覆うひとつながりの器官でありながら、変態中のおたまじゃくしの皮膚は成体化した胴体と幼生型のままの尾の境目がはっきりしている。例えていうなら、上半身がヒトで下半身が魚の人魚姫のようだ。
(註1) MHC(Major Histocompatibility Complex: 主要組織適合性複合体)
免疫反応に必要な一群のタンパク質の複合体。免疫系は自己と非自己を厳格に識別するが、この識別は細胞表面に存在する一群のタンパク質によって、Tリンパ球に抗原が提示されることによって起こる。MHCは多型性に富むことでよく知られており、ヒトのMHCはヒト白血球型抗原、 HLA (Human Leukocyte Antigen)と呼ばれ、臓器移植の際の拒絶反応の起こりやすさにはHLA型の多型による相性が大きく関わる。
2.カエルの免疫系はおたまじゃくしの尾を自己と見なすか?
学生時代の私は、あらゆる器官が幼生型から成体型へ変わる変態期に、尾の皮膚だけ変わらないことに注目し、MHCが完全に同一なアフリカツメガエルのJストレイン(註2)のおたまじゃくしの尾の皮膚を切り取り、変態したての同系統のカエルに移植した。この実験は「子供のころに採取し保存しておい自分の組織を、第二次性徴期を終えて成熟した大人になってから移植した時、その細胞を免疫が“異物”として認識するか」という問いに相当する。結果は拒絶であった(図3)。成体同士の交換移植は生着する(拒絶されず己の皮膚として生き続ける)にもかかわらずである。興味深いことに、変態初期の幼生の皮膚はすべて成体から拒絶されるのに、変態末期の幼生では胴体の皮膚は生着し、尾の皮膚だけが拒絶される。
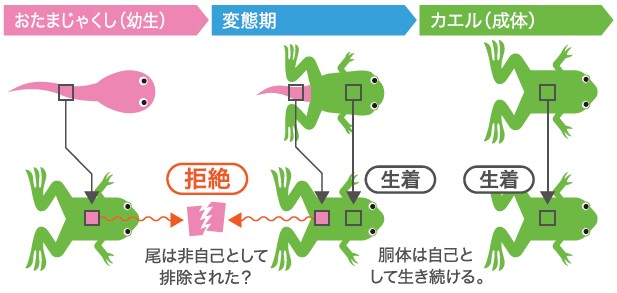
(図3) Jストレインを使った移植実験
幼生皮膚の拒絶反応には二次応答が起きる。二次応答とは同じホスト(この場合若いカエル)に同じ移植を繰り返すと体の中に抗体が産生され、それによって拒絶反応が早まる現象で、免疫応答の特徴のひとつである。予防接種で抗体をつくり、ウィルスを排除できるようにするのはこの反応を利用している。
これらの結果から私は「おたまじゃくしの尾は変態期に成体の免疫細胞に拒絶されて消失する」という仮説をたてた。両生類の変態研究の歴史の中で長く続いてきたホルモン説に対する約100年ぶりの新説である。免疫が動物の体づくりにも関わっているのではないかということは誰も考えたことがなかったので、魅力的な課題だった。
(註2) Jストレイン
30代以上近親交配を繰り返すことによって得られた完全にMHCが同一な系統で、世界で唯一の近交系両生類である。日本で樹立されたために、JapanのJをとってその名が付けられた。互いに交換移植が可能なため、免疫系の発生を明らかにする上で数々の有用な実験系を提供してきた。
3.免疫細胞が尾を壊す時の目印を探す
免疫と尾の消失との関わりを明らかにするために、まず免疫細胞のひとつであるTリンパ球のはたらきを見た。Tリンパ球は試験管内で異物に出会うと増殖する。つまり、Tリンパ球の増殖反応の有無で相手を異物として認識しているかどうかがわかる。切り取ったJストレインのおたまじゃくしの尾の組織を培養し、そこへ同系統の成体のTリンパ球を加え5日間培養したところ、予想通り増殖した。一番知りたかったのは、尾が縮み始めた変態末期の幼生の体の中にあるTリンパ球の尾の皮膚に対する反応だ。この場合も増殖した。これらの結果から、成体のTリンパ球は尾を異物として認識すること、しかも「尾を異物として認識する能力のあるTリンパ球」がおたまじゃくしの体の中に変態期に既に出現していることがわかった。
次に私たちは、尾が異物として認識される時の目印、つまり抗原となるタンパク質を探した。先に述べた二次応答の時にできる抗体を利用して、おたまじゃくしの皮膚に含まれるたくさんのタンパク質の中から、2つの抗原タンパク質を選別・同定し、それぞれをつくる遺伝子を特定したところ、ケラチン(註3)の一種であることがわかった。ツメガエルでは皮膚を構成するケラチンに幼生型と成体型の2種類が既に知られているが、私たちが見出したものはそれらとは異なる新しいケラチンであった。尾を自ら壊す時の目印となることから、古代ギリシャ語で「己の尾を食らう空想上の生きもの」を意味するOuroboros(オウロボロス、またはウロボロス)から、それぞれouro1,ouro2と命名した。
(註3)ケラチン
ヒトでは皮膚細胞、爪や毛の主成分となっており、細胞骨格を構成するタンパク質の一つである。
4.オウロボロス遺伝子のはたらきを見る
ouro遺伝子は若い胚の時期には発現せず、変態期に入ると2つそろって全身で弱く発現し、変態最盛期には胴体での発現が消える。一方、尾では2つそろって発現量が増え続け、尾の退縮が完了するまでピーク時の値のまま残る。
では、遺伝子の発現時期を早くすれば、尾の退縮も早まるだろうか。それを知るために、ouro遺伝子にGFP(註4)をつなぎ、熱を加えた場合にのみ発現を開始するヒートショックプロモーターの下流に組み込んだ。これで、遺伝子がいつ・どこで発現するかを限定できる(図4)。まだ尾が縮む前のおたまじゃくしの尾の先端部分に、ouro1とouro2を過剰発現させたところ、通常は10~14日かけて縮む尾が、なんと4日間で崩壊し(図5)、そこにTリンパ球が集積していた。ところが、ouro1もしくはouro2片方だけの過剰発現では尾は崩壊しなかった。つまり、ouro1とouro2の両方の発現がないと尾は崩壊しない。これは実際の尾においても2つそろって発現することとも一致する。
次に、アンチセンス法(註5)を用いてouro遺伝子の機能を阻害したところ、ouro1もしくはouro2どちらか片方だけの阻害によって尾の一部が残った(図6)。過剰発現の実験結果とも合致した。従って、2種類のouro遺伝子の発現が尾の消失に不可欠であると結論した(図7)。

上:(図4) 発現調節実験の様子
下:(図5)オウロボロス遺伝子の発現を早める実験

(図6)オウロボロス遺伝子の発現を抑える実験
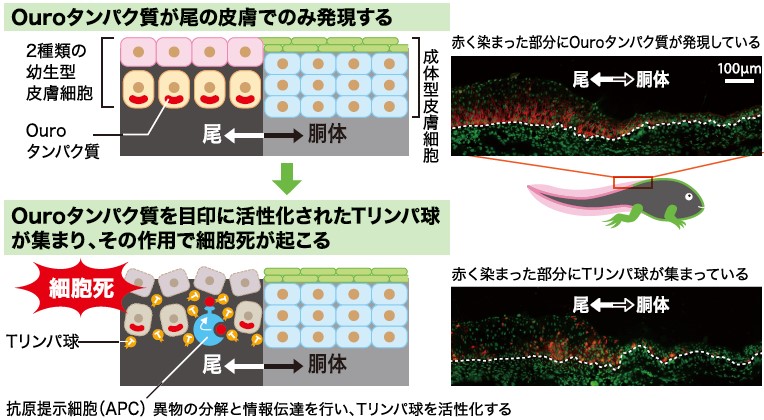
(図7) 免疫細胞がかかわる尾の消失のしくみ
(註4)GFP(Green Fluorescent Protein: 緑色蛍光タンパク質)
オワンクラゲから発見された蛍光タンパク質。発現している箇所が緑色に光るため、目的の遺伝子が発現しているかどうかを確認するための目印として導入されることが多い。図5(実際に光っている写真)を参照。
(註5)アンチセンス法
相補的な配列をもつ分子は互いに結合して二本鎖となる、という性質を利用して、逆向きのDNA配列を過剰発現させ、内在性の既に発現しているRNAと相補的に結合することで二本鎖とさせ、本来は一本鎖ではたらくRNAのタンパク質合成を阻害する手法。
5.体づくりと免疫の関わり-新しい概念の確立にむけて
私たちの研究は、単におたまじゃくしの尾の消失に関わるしくみを明らかにしただけではなく、これまで生体防御のしくみとだけ考えられていた免疫が体づくりに関わるという新しい機能を示すものである。変態末期に一過的にしか上昇しないホルモンではなく、一度経験したことを「記憶」する免疫を利用することで、いらなくなった細胞を排除し続けることが体づくりに必要なのかもしれない。
ouro遺伝子は、両生類だけではなく、相同な遺伝子は魚類などさまざまな動物がもっていることがわかっている。今後はそれらの機能も解析し、ouro遺伝子を発現する細胞が免疫系から非自己として積極的に排除されるか否かを見ていきたい。免疫がかかわる全か無かの認識機構が、体づくりのしくみにも関わっているという一般解が得られるのではないかと期待している。

井筒ゆみ(いづつ・ゆみ)
1988年東京都立大学理学部生物学科卒業。1993年広島大学大学院理学研究科修了。博士(理学)。JSPS(日本学術振興会)特別研究員、北海道大学免疫科学研究所助手、新潟大学大学院自然科学研究科助手などを経て2006年より同大学理学部生物学科助教。現在、准教授。
![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)



.jpg)
.jpg)










.png)