Experiment
電子線で膜たんぱく質を観る
DNAの二重らせん構造の見事さに感動した人は少なくないだろう。
生き物にとってDNAと同じくらいたいせつなたんぱく質も、ミクロのレベルで見ると、その精緻で巧妙な構造は芸術作品といえるほど美しい。
原子レベルの解析のために開発された最新の電子顕微鏡で見る1000万分の1ミリの世界。
「百聞は一見にしかず」は使い古された格言だが、それだけに人間の認識の中心がどこにあるかを言い得ていると思う。生命の営みの中心的な役割を担うたんぱく質の機能にしても、その精繊な構造を“観る”ことによって、よりよく理解できる。
物質の構造を調べる結晶学は、イギリスの物理学者のW. H. BraggとW. L. Bragg父子が1912年に基礎を作った。なかでもX線を使って実験を行なうX線結晶学とその周辺の学問の進歩はめざましく、いまや毎日新しいたんぱく質の構造が解析され発表されるようになっている。しかし、細胞や生体それ自身が、外部との情報やエネルギーをやりとりするのに欠かせない膜たんぱく質(細胞膜や細胞小器官の膜の上にあるたんぱく質のこと)については、3次元の大きい結晶を成長させられないために、X線結晶学による解析が難しい。
X線の1万倍以上の散乱能をもつ電子線を用いれば、たった1枚の薄い膜(厚さ約50Å。1Åは1000万分の1mm)からでもたんぱく質の構造についての情報を取り出せることは古くから言われていた。それなら、X線結晶学に代わる電子線結晶学ができそうなものだが、私が電子顕微鏡学を習いはじめた1973年当時は、電子顕微鏡で原子が見えるかどうかさえ不明だった。塩化フタロシアニン銅の結晶を使ってはじめて原子を分離した形で分子構造を撮影できたときの、足がふるえるような感動は15年を経たいまでも覚えている(写真①)。これで原子レベルでの構造解析が可能であることは確認できた。しかし、生体試料は電子線を少し当てただけでも壊れてしまうために、塩化フタロシアニン銅のような高分解能像は撮影できなかった。
必要最小限の電子線の照射で撮影ができる新しい装置を1980年に開発したが、原子レベルでの構造解析には、試料の電子線による損傷をさらに桁違いに減らす必要があった。そのためには、試料を絶対0度(-273.16℃)に近い極低温に冷やす以外にないことが明らかになった。だが、高分解能像を撮影できる極低温ステージ開発の試みは、冷媒が振動するためにことごとく失敗していた。
1983年に始まったわれわれの極低温電子顕微鏡の開発(京都大学山岸秀夫博士らと日本電子との共同研究)も、娘の保育園の遠足で低温物理学者水崎隆雄博士(京都大学理学部)に出会い、教えを受けることができなければ確実に失敗していたと思う。1台が数億円という高価な装置を、開発を始めてから11年の間に改良を重ね、3号機までを作ることができた。こうして、たんぱく質の電子線損傷を1桁以上減らして、絶対温度1.5K(-271.7℃)で分解能2Åの極低温電子顕微鏡を作ることができたのである。
しかし、たんぱく質の構造解析には、これだけでは十分ではない。1枚の電子顕微鏡像では2次元の像しか得られないので、試料をいろいろな方向に傾けて撮影することが必要になる。いろいろな角度で撮影した像のデータを200枚程度使って電子密度図をコンピュータで計算、これをもとにアミノ酸配列に合うように構成原子の位置を決めると、最後にたんぱく質の立体構造が見えてくるのである。
私たちが、最初に解析に成功したのは、ソラマメの葉の葉緑体の膜内で、光合成に使われる光エネルギーを効率よく集めるはたらきをするアンテナたんぱく質である。このたんぱく質は膜の中に密に配列し、光のエネルギーの伝搬に都合がよいように3つの分子が集まった3量体を形成している。私たちは、アンテナたんぱく質中に、光合成反応に必要なクロロフィルなどの機能性分子がどのような配置をしているかを、原子のレベルで明らかにすることができた。その結果、アンテナたんぱく質が、2種類のクロロフィル(aとb)とルテインと呼ばれる補助色素をじつにうまく配置させ、そのおかげで光のエネルギーを効率よく伝搬するとともに、光に当たって活性化されたクロロフィルaが光合成反応で発生する酸素に触れて壊れてしまうのを防いでいることがわかった。
電子線を使って研究を始めてから、ほぼ20年。やっと電子顕微鏡でたんぱく質の構造を原子レベルで解析できるようになった。現在の解析システムでは、一つのたんぱく質の構造を決めるのにまだ2年程度かかるが、これをさらに良いものにし、膜たんぱく質の動的な構造を次々に解析できるようにするのが近い将来の夢である。

塩化フタロシアニン銅結晶の分子像。電子顕微鏡で原子が見えることをはじめて証明した歴史的像
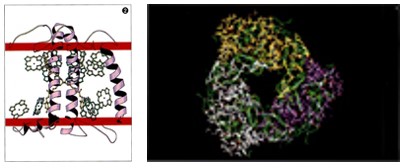
(左)ソラマメの葉にある光合成のアンテナたんぱく質の立体構造図。紫のリボン-たんぱく質のらせん部分、緑一クロロフィルa、黄緑一クロロフィルb、黄一ルテイン
(右)アンテナたんぱく質の構造。同一の分子が3つ集まって3量体を作っている
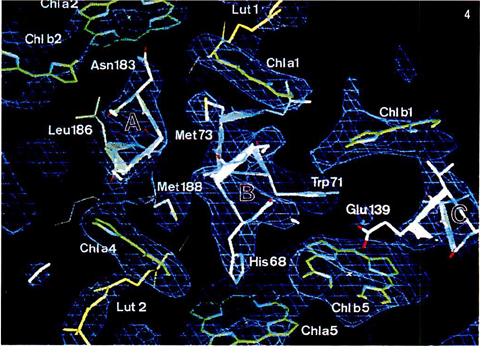
コンピュータで計算した電子密度図(図で網状に見える部分)に合わせてアミノ酸を原子のレベルで配置したもの(Nature, 1994年, 第367巻, 616ページより)
(ふじよし・よしのり/蛋白工学研究所首席研究員)
※所属などはすべて季刊「生命誌」掲載当時の情報です。![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)


.jpg)

.jpg)
.jpg)









.png)