RESEARCH
女王を育むロイヤラクチン
ミツバチの巣には、数十匹のオス蜂と数万匹のメスの働き蜂、そして1匹の女王蜂が暮らしています。女王蜂は働き蜂に比べて体が1.5倍、寿命は20倍、1日に卵を2000個も産みます。女王蜂と働き蜂の遺伝子型は同じなのに、ローヤルゼリーを食べて育った幼虫だけがこの能力をもつのです。これは100年も前から知られていましたが、ローヤルゼリーの中の何が、どのようにして女王蜂を育むのかは謎のままでした。
この謎に挑んだ富山県立大学の鎌倉昌樹さんは、ローヤルゼリーの中のロイヤラクチンというタンパク質が鍵物質であることを解き明かしました。この先が驚きです。ロイヤラクチンをショウジョウバエに与えたところ、女王バエが生まれたのです。ここから何が解けるのか。新しい研究の始まりです。
1.女王蜂を育むローヤルゼリー
ミツバチの巣には、数十匹のオス蜂と数万匹のメスの働き蜂、そして1匹の女王蜂が暮らしている。オス蜂は未受精卵から生まれ、メスの働き蜂と女王蜂は受精卵から生まれる。メスの働き蜂と女王蜂はまったく同じ遺伝子をもっているが、通常の巣房でハチミツや花粉を摂取して育ったものは働き蜂へ、王台という女王専用の部屋でローヤルゼリーを摂取したものは女王蜂へと分化する(図1)。このように、女王蜂への分化はローヤルゼリーによって後天的(エピジェネティック(註1))に誘導されることははっきりしているのだが、ローヤルゼリーの中の何が分化誘導の鍵を握っているかは不明だった。また、ローヤルゼリーによる分化誘導には、幼虫で高濃度に分泌され成長を促す幼若ホルモン(註2)が関わるのだが、これについても作用の詳細は不明だった。そこで私は、女王蜂への分化を誘導するローヤルゼリー中の因子の特定と、それがもたらす分化誘導のメカニズムの解明に挑んだ。
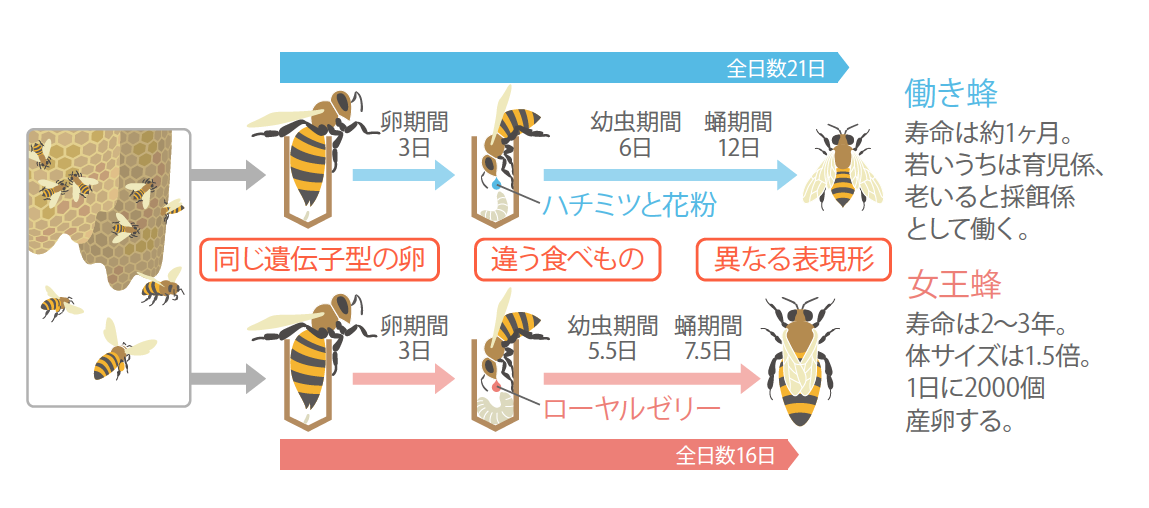
(図1) 働き蜂と女王蜂の生活環
働き蜂と女王蜂は同じ遺伝子型の卵から生まれるにも関わらず、違う食べ物を摂ることによって、異なる表現型の成虫へと変態する。女王蜂は働き蜂よりも体サイズが大きいにも関わらず、幼虫と蛹の期間は働き蜂のそれよりも短い。
(註1) エピジェネティック
DNAの塩基配列の変化を伴わずに、遺伝子の発現を制御する現象。
(註2) 幼若ホルモン
昆虫ホルモンの一種。昆虫の頭部にあるアラタ体から分泌され、幼虫の成長を促す。
2.ローヤルゼリーから見つかったロイヤラクチン
ローヤルゼリー中の因子が特定できなかった理由の1つは、働き蜂に分化させる培地がなかったためである。その培地があれば、ローヤルゼリーにある候補因子を培地に加え、どのような蜂になるかを観察すればよい。そこで、まず働き蜂に分化させる培地を探索した。ミツバチの研究を始める以前に、新鮮なローヤルゼリーはマウスで抗疲労効果を示すが、40℃で7日間保存したローヤルゼリーはその効果がないことを明らかにしていた。そこで、ミツバチに40℃で7日間保存したローヤルゼリーの培地を試したが、女王蜂への分化の指標が若干減少しただけだった。保存期間を延長し、14日間、21日間、30日間のローヤルゼリーを試したところ、40℃で30日間保存したローヤルゼリーが完全に働き蜂を誘導した(図2)。これで実験が出来る。研究とはこのような地道な下積みの積み重ねなのである。この培地を用いて女王蜂への分化誘導因子を探した。
新鮮なローヤルゼリーと40℃で30日間保存したローヤルゼリーのタンパク質を比較したところ、後者では57kDa(註3)、170kDaのタンパク質がほぼ失われ、450kDaのものは著しく減少した。女王蜂への分化誘導の能力は、この中のロイヤラクチンと命名した57 kDaのタンパク質だけに存在した(図2)。さらに、大腸菌を用いて生成した組換えロイヤラクチンを与えた場合も、女王蜂への分化誘導を確認した。ロイヤラクチンはまた、幼虫期の幼若ホルモンの分泌を促進した。こうして、ローヤルゼリー中に含まれる女王蜂への分化誘導因子はロイヤラクチンであることが明らかになった。
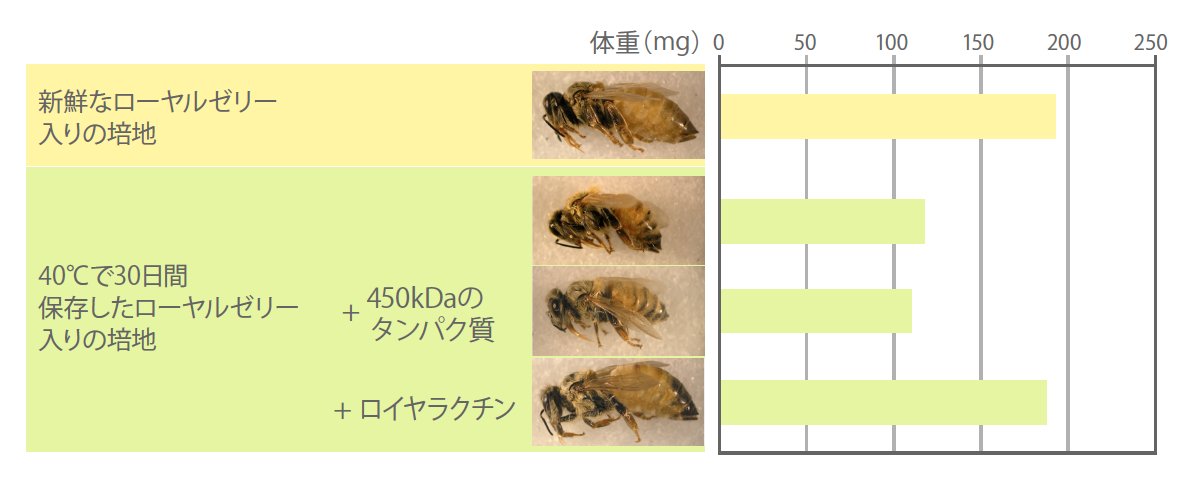
(図2) 働き蜂を分化誘導する培地とロイヤラクチンの効果
40℃で30日間保存したローヤルゼリー入りの培地で飼育することによって、働き蜂を分化誘導することができた。ローヤルゼリー中にある450kDaのタンパク質を摂取した個体は女王蜂に分化しなかったが、57kDaのロイヤラクチンを摂取した個体は女王蜂に分化した。
Kamakura, M., Nature, 473, 478~483 (2011) より改変
(註3) Da (ダルトン)
質量の単位。1Daは炭素原子(12C)の質量の1/12と定義され、数値的には分子量と同じである。
3.ロイヤラクチンの作用が種を超えた
因子は明らかになったが、ミツバチには実験に使える変異体がないので、分化誘導の分子メカニズムの解析ができない。もし、ショウジョウバエでロイヤラクチンの効果が認められれば、その変異体を用いて実験が進められるはずである。ローヤルゼリーだけを与えたのではショウジョウバエは死んでしまったが、培地の組成を変えて検討した結果、体サイズを増加させるローヤルゼリー入りの培地を作ることができた(図3左)。この培地を用いてショウジョウバエに対するロイヤラクチンの効果を調べたところ、ミツバチと同様に、ロイヤラクチンが体サイズ、産卵数、寿命の増加を誘導した。このような変化は、Gal4/UASシステム(註4)を用いて、ショウジョウバエの体内でロイヤラクチンを過剰に発現させた場合にもみられた(図3右)。種をこえてロイヤラクチンが作用するとは驚くべき結果である。これは、生育環境によって形質が変化する現象が、生物に普遍的に存在することを示唆している。

(図3) ショウジョウバエに対する効果
(左) カゼイン入りの培地で飼育したショウジョウバエと比べて、ローヤルゼリー入りの培地で飼育した個体は体サイズが増加した。カゼイン培地は、ローヤルゼリーと同等のエネルギー摂取量になるよう調製したもの。
(右) 普通のハエと比べて、脂肪体でロイヤラクチンを過剰発現させた系統は体サイズが増加した。
Kamakura, M., Nature, 473, 478~483 (2011) より改変
(註4) Gal4/UAS システム
特定の器官で目的とするタンパク質を発現させるシステム。特定の器官で発現するタンパク質のプロモータの下流に転写因子をコードするGal4遺伝子を挿入することによって、発現したGal4がエンハンサ−配列のUASに結合し、その近傍の遺伝子を活性化して目的とするタンパク質を発現させる。
4.EGFRから始まる反応カスケード
次に、様々なショウジョウバエの変異体を用いて、ロイヤラクチンによる分化誘導機構を解析した。これまでは、生物の体サイズや寿命などの制御には、インスリン受容体(註5)が中心的な役割を担っているとされてきた。ところが、摂取されたロイヤラクチンは哺乳類の肝臓に相当する脂肪体に移行し、脂肪体の細胞膜上にある上皮成長因子受容体(EGFR:epidermal growth factor receptor)(註6)に作用することで女王蜂への分化を誘導していたのである(図6)。
EGFRから伝わったシグナルはS6キナーゼ(註7)を介して細胞の大きさを増加させ、その結果、個体サイズが大きくなった(図4, 6)。
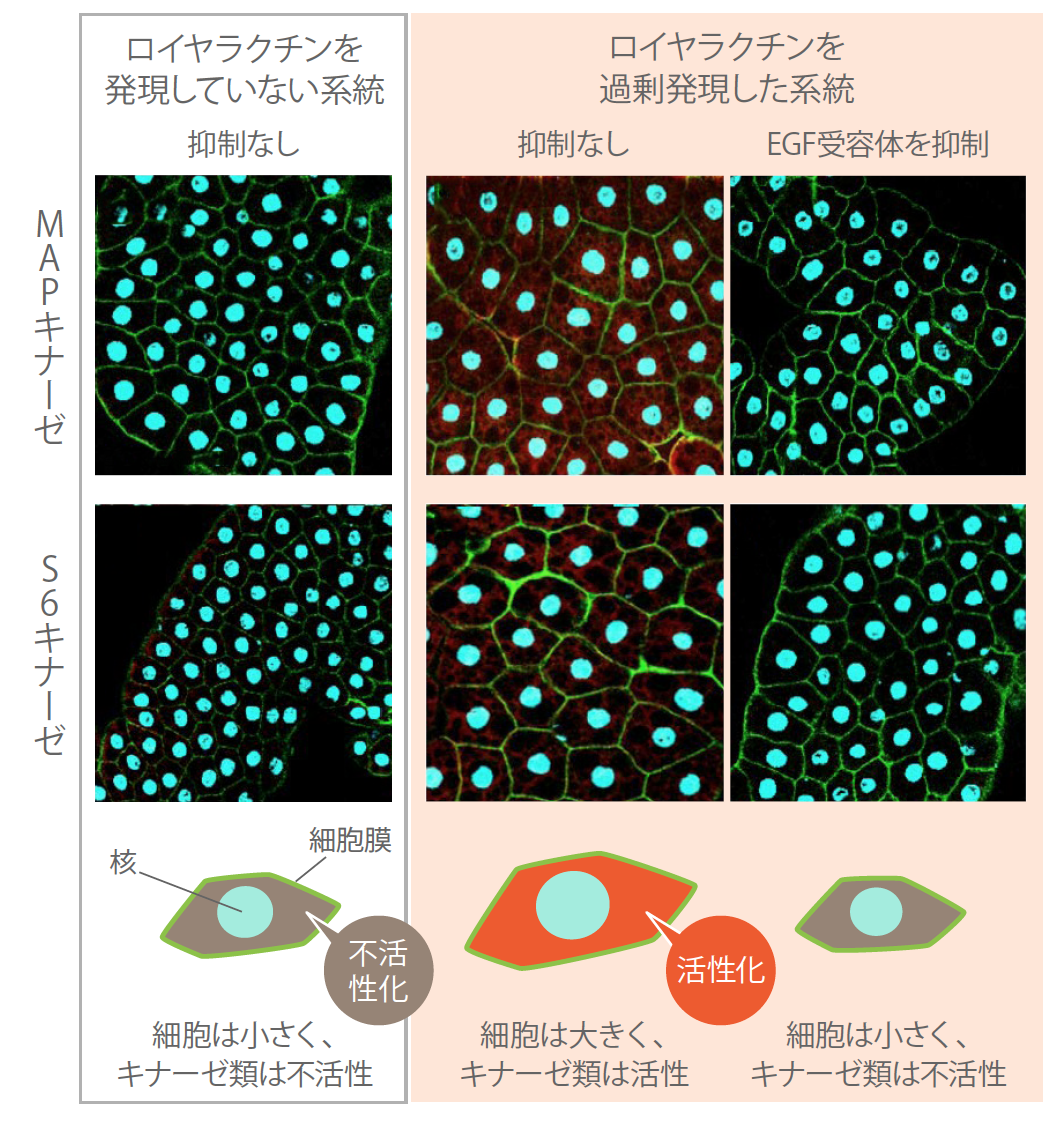
(図4) 脂肪細胞におけるキナーゼの活性化
脂肪体にロイヤラクチンを過剰発現させた系統では、細胞内に赤色の信号がみられ、どちらのキナーゼも活性化するとともに脂肪細胞のサイズが増加した。この系統に対してEGF受容体の発現を抑制した場合、どちらのキナーゼも活性が抑制された。
Kamakura, M., Nature, 473, 478~483 (2011) より改変
生物は一般的に、体のサイズが大きいものほど発生期間が長いが、女王蜂は働き蜂に比べて体が大きいにも関わらず早く羽化する。この特徴はショウジョウバエにロイヤラクチンを与えた場合、あるいは過剰に発現させた場合にも観察された。これは、ロイヤラクチンがEGFRを介してMAPキナーゼ(註8)を活性化し、脱皮ホルモンの分泌を増加させることに起因していた(図4, 6)。女王蜂への分化誘導のための重要な内因性因子である幼若ホルモンについても、ロイヤラクチンはミツバチとショウジョウバエともに、EGFRを介してその分泌を誘導する。幼若ホルモンはその受容体と結合し、卵黄タンパク質(註9)の発現を増加させ、産卵数の増加に関与していた(図6)。さらに興味深いことに、EGFRからのシグナルは寿命の延長にも関わっていることが初めて見いだされた(図6)。ショウジョウバエで明らかになった以上の機構をミツバチでも確認するために、RNAi(註10)試験を中心に詳細な解析を行った。その結果、ミツバチでもロイヤラクチンがEGFRを介して女王蜂への分化を誘導することが確かめられた(図5)。

(図5) ミツバチにおけるRNAi試験
インスリン受容体の発現をRNAiで抑制した場合は女王蜂に分化誘導したが、EGF受容体あるいは体サイズの増加に関係するS6キナーゼを抑制した場合は、顕著に体重が減少した。GFPのRNAiによる抑制は、比較対象群。
Kamakura, M., Nature, 473, 478~483 (2011) より改変
(註5) インスリン受容体
インスリンと結合する細胞膜にあるタンパク質。インスリンとの結合によって、細胞内へグルコースを取り込み、タンパク質の合成を促進する。
(註6) 上皮成長因子受容体(EGFR)
上皮成長因子(EGF)と結合する細胞膜にあるタンパク質。EGFとの結合によって、細胞の増殖や分化のためのシグナルを送る。
(註7) S6キナーゼ
リン酸化によって活性化されるセリン-スレオニンキナーゼの一種。リボソームタンパク質S6をリン酸化することによって、特定のタンパク質の合成を高める。
(註8) MAPキナーゼ
リン酸化によって活性化されるセリン-スレオニンキナーゼの一種。細胞の増殖や分化を制御する細胞内シグナル伝達の中心的な役割を果たす。
(註9) 卵黄タンパク質
卵母細胞内にあるタンパク質。多くは前駆体として肝臓で合成され、血中に分泌された後に卵巣で卵母細胞内に移行する。
(註10) RNAi
2本差RNAを細胞内に導入することにより、標的とするmRNAを分解することによって、特定のタンパク質の合成を抑制する方法。
5.さらに広がるミツバチ研究
ローヤルゼリーの中からメスのミツバチを女王蜂へと分化誘導する因子としてロイヤラクチンを見いだすことができた。そして、ロイヤラクチンのEGFRシグナルを介した女王蜂への分化誘導機構の詳細を明らかにすることができた(図6)。これらの結果は、今後のミツバチ研究を飛躍させる大きな一歩である。ここから、生殖活動を1匹の女王蜂と少数のオス蜂のみに託す超個体としての生物集団として存在するハチやアリなど膜翅目特有の階級社会の進化上の謎に近づけるだろう。今後は、ミツバチの脳における神経系の発生分化のメカニズムを解明したい。それによって、ミツバチの行動と脳の構造との関係性を明らかにし、ミツバチの社会性の謎に迫りたい。ミツバチの脳に関する研究は、さらに、いま深刻な問題となっている蜂群崩壊症候群(註11)の解明にもつながると考えている。また、ロイヤラクチンで分化誘導した女王蜂が実際にコロニーで機能すれば、ここで開発したin vitro飼育系を女王蜂の安定供給に活用できるだろう。
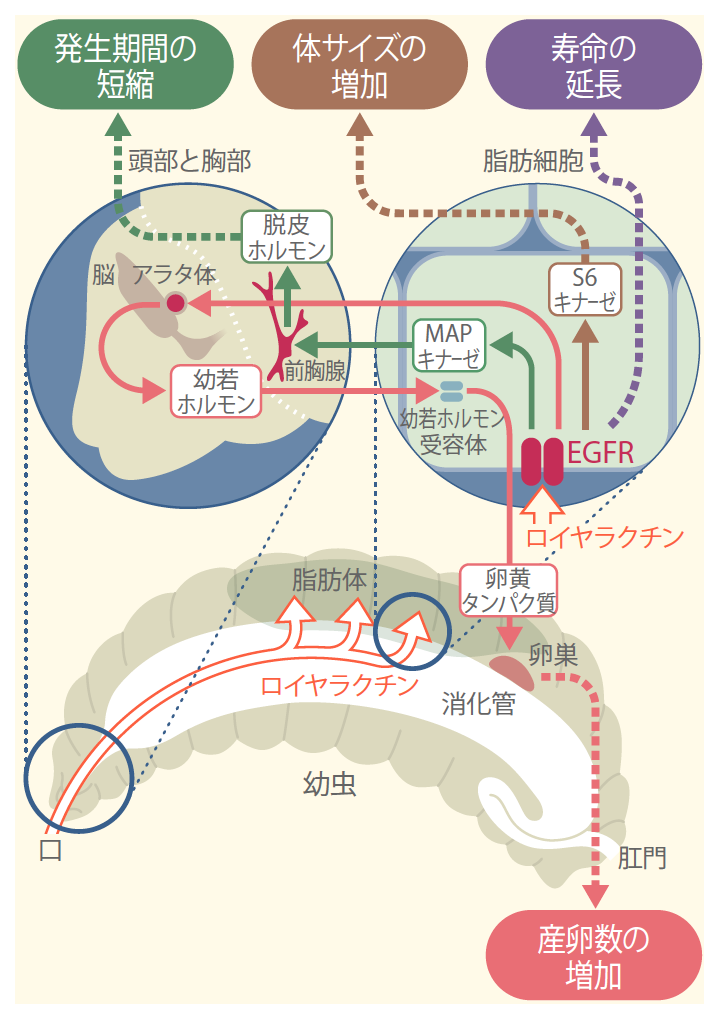
(図6) ロイヤラクチンによる女王蜂への分化誘導の分子メカニズム
口から取り込まれたロイヤラクチンは、幼虫の脂肪体にある脂肪細胞表面のEGFRに作用する。EGFR からの信号は前胸腺や卵巣に伝わり、女王蜂の特徴が現れる。この図では、ショウジョウバエで確かめられた詳細をミツバチの幼虫として表現した。
(註11) 蜂群崩壊症候群
ミツバチが短期間に大量に失踪する現象。原因は特定されていない。

鎌倉昌樹(かまくら まさき)
1996年京都大学大学院農学研究科修了。天野製薬株式会社研究員、ポーラ化成工業株式会社研究員を経て、2008年より富山県立大学工学部生物工学センターおよび生物工学科講師。
![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)



.jpg)
.jpg)










.png)