ラボ日記
2026.03.03
構造解析におけるコンタミ
小田研の津山です。ショウジョウバエカドヘリン細胞外部分の立体構造を解き明かす、というプロジェクトを引き続き進めています。今回は、最近その構造解析の中で出くわした”コンタミ”について書きます。
生物学系の研究者はよく”コンタミ”という言葉を使います。これは英語のcontaminationあるいはcontaminantに由来するカタカナ英語だと思われ、目的のものに対して、目的のものではないもの、が混入してしまったような場合に使います。特に混ざった結果として問題が起こるような場合に使われることが多く、例えば、飼育している生物や細胞に別の生物や細胞が混じってしまう場合などに。私が以前ショウジョウバエを扱っていたときに、よくあったのはカビのコンタミです。通常の飼育温度ではハエの方が元気なのでカビはあまり増えてこないのですが、温度を下げていると時々カビが増えていきます。カビは餌の表面で増殖するため、カビが増えすぎると成虫が餌を食べられない、あるいは幼虫が餌から出られない、という状況になります。そうすると、貴重なハエ系統を助けるためにちょっとした救助活動的な作業が必要になったり、努力も虚しく系統を失ってしまったりということになるため、ハエへのコンタミはかなり困った問題でした。
タンパク質の構造解析でもコンタミは起こります。この場合、構造を決めたいと考えている目的タンパク質の試料に、別の種類のタンパク質が混入することが多いです。タンパク質の構造を決めるためには高純度のタンパク質試料、つまり目的タンパク質の割合が高い試料が必要になります。タンパク質の構造解析は、多くの場合、培養細胞で目的タンパク質を発現 (合成) させることから始まりますが、この細胞は目的タンパク質以外も発現しています。ここから精製と呼ばれる過程でいくつかの方法を組み合わせて、目的タンパク質の割合が高い試料を取得しますが、実際には、不要なタンパク質をすべて除くということは当然不可能です。また、精製に使った実験材料の中のタンパク質が混入する場合もあります。こういった目的のものではないタンパク質やその影響が構造解析で見えてくると、コンタミと呼ばれるようになります。このようなコンタミはよくあることらしく、タンパク質の結晶解析で見つかった、コンタミタンパク質のデータベースを作ったことを報告している論文もあるほどです (引用1)。
そういうわけで、構造解析をしていると、コンタミと時々遭遇します。下は以前、ヒトに由来する培養細胞からヒト膜タンパク質 (トランスポーター) を精製して、構造解析しているときに出てきた、コンタミタンパク質粒子の画像 (正確にはたくさんの粒子の2次元平均像) です。

ここには2種類のコンタミタンパク質が含まれており、赤枠で囲んだ画像は形から判断しておそらくプロテアソームと呼ばれる、非常に有名なタンパク質複合体です。筒状の形をしており、2つの画像は観察された時の向きが違います。それ以外については見た目だけではわからなかったのですが、少し解析してみただけでそれなりの分解能で3次元構造を決定することができ、protein arginine N-methyltransferase (PRMT) 5とmethylosome protein 50 (MEP50) と呼ばれるタンパク質から構成されたタンパク質複合体であることがわかりました。必死に解析した目的のトランスポーターは分解能がイマイチで、当初の目的は果たせませんでした。それでもPRMT5/MEP50の構造がこれまで知られていないものなら論文として公表できて、ちょっとしたセレンディピティ的なストーリーになるところでしたが、すでに構造は報告されており (引用2)、そんな都合のいい話にはなってくれませんでした。
そして、最近出くわした、ハエの細胞から精製された、ハエのカドヘリンの構造解析でのコンタミタンパク質の画像が下です。
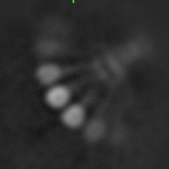
画像右上の軸となる部分から、先端が丸くなった腕のような構造がたくさん伸びており、かなり変わった形の分子です。最初目にしたときにはこれがタンパク質かどうかすらよくわかりませんでしたが、形の特徴から調べた結果、C1qと呼ばれる脊椎動物の免疫系で働いているタンパク質複合体らしいということがわかりました (引用3)。ということは、ハエのカドヘリンタンパク質をハエの細胞から取ってきたのに、脊椎動物のタンパク質が出てきたということになります。これだけ書くと不思議なことのように思えますが、原因はおそらく単純です。細胞の培養液には牛の血清が添加されており、その中に含まれていたC1qがコンタミしたと考えられます。低温電子顕微鏡を使った構造解析では、形が似ているタンパク質粒子をグループとしてまとめて分けていくので、これだけ形が特徴的なら、C1qの存在は我々の目的タンパク質の構造解析ではあまり問題にはならない可能性が高いです。今回の日記のネタにもなってくれて、これまで出くわした多数のコンタミの中で、一番良いコンタミといえるかもしれません。
引用1
Hungler, A., Momin, A., Diederichs, K. & Arold, S., T. ContaMiner and ContaBase: a webserver and database for early identification of unwantedly crystallized protein contaminants. J. Appl. Crystallogr. 49, 2252–2258 (2016). https://pmc.ncbi.nlm.nih.gov/articles/PMC5140001/
引用2
Antonysamy, S. et al. Crystal structure of the human PRMT5:MEP50 complex. Proc. Natl. Acad. Sci. 109, 17960–17965 (2012). https://pubmed.ncbi.nlm.nih.gov/23071334/
引用3
Bally, I. et al. Expression of recombinant human complement C1q allows identification of the C1r/C1s-binding sites. Proc. Natl. Acad. Sci. 110, 8650–8655 (2013). https://pmc.ncbi.nlm.nih.gov/articles/PMC3666734/
生物学系の研究者はよく”コンタミ”という言葉を使います。これは英語のcontaminationあるいはcontaminantに由来するカタカナ英語だと思われ、目的のものに対して、目的のものではないもの、が混入してしまったような場合に使います。特に混ざった結果として問題が起こるような場合に使われることが多く、例えば、飼育している生物や細胞に別の生物や細胞が混じってしまう場合などに。私が以前ショウジョウバエを扱っていたときに、よくあったのはカビのコンタミです。通常の飼育温度ではハエの方が元気なのでカビはあまり増えてこないのですが、温度を下げていると時々カビが増えていきます。カビは餌の表面で増殖するため、カビが増えすぎると成虫が餌を食べられない、あるいは幼虫が餌から出られない、という状況になります。そうすると、貴重なハエ系統を助けるためにちょっとした救助活動的な作業が必要になったり、努力も虚しく系統を失ってしまったりということになるため、ハエへのコンタミはかなり困った問題でした。
タンパク質の構造解析でもコンタミは起こります。この場合、構造を決めたいと考えている目的タンパク質の試料に、別の種類のタンパク質が混入することが多いです。タンパク質の構造を決めるためには高純度のタンパク質試料、つまり目的タンパク質の割合が高い試料が必要になります。タンパク質の構造解析は、多くの場合、培養細胞で目的タンパク質を発現 (合成) させることから始まりますが、この細胞は目的タンパク質以外も発現しています。ここから精製と呼ばれる過程でいくつかの方法を組み合わせて、目的タンパク質の割合が高い試料を取得しますが、実際には、不要なタンパク質をすべて除くということは当然不可能です。また、精製に使った実験材料の中のタンパク質が混入する場合もあります。こういった目的のものではないタンパク質やその影響が構造解析で見えてくると、コンタミと呼ばれるようになります。このようなコンタミはよくあることらしく、タンパク質の結晶解析で見つかった、コンタミタンパク質のデータベースを作ったことを報告している論文もあるほどです (引用1)。
そういうわけで、構造解析をしていると、コンタミと時々遭遇します。下は以前、ヒトに由来する培養細胞からヒト膜タンパク質 (トランスポーター) を精製して、構造解析しているときに出てきた、コンタミタンパク質粒子の画像 (正確にはたくさんの粒子の2次元平均像) です。

ここには2種類のコンタミタンパク質が含まれており、赤枠で囲んだ画像は形から判断しておそらくプロテアソームと呼ばれる、非常に有名なタンパク質複合体です。筒状の形をしており、2つの画像は観察された時の向きが違います。それ以外については見た目だけではわからなかったのですが、少し解析してみただけでそれなりの分解能で3次元構造を決定することができ、protein arginine N-methyltransferase (PRMT) 5とmethylosome protein 50 (MEP50) と呼ばれるタンパク質から構成されたタンパク質複合体であることがわかりました。必死に解析した目的のトランスポーターは分解能がイマイチで、当初の目的は果たせませんでした。それでもPRMT5/MEP50の構造がこれまで知られていないものなら論文として公表できて、ちょっとしたセレンディピティ的なストーリーになるところでしたが、すでに構造は報告されており (引用2)、そんな都合のいい話にはなってくれませんでした。
そして、最近出くわした、ハエの細胞から精製された、ハエのカドヘリンの構造解析でのコンタミタンパク質の画像が下です。

画像右上の軸となる部分から、先端が丸くなった腕のような構造がたくさん伸びており、かなり変わった形の分子です。最初目にしたときにはこれがタンパク質かどうかすらよくわかりませんでしたが、形の特徴から調べた結果、C1qと呼ばれる脊椎動物の免疫系で働いているタンパク質複合体らしいということがわかりました (引用3)。ということは、ハエのカドヘリンタンパク質をハエの細胞から取ってきたのに、脊椎動物のタンパク質が出てきたということになります。これだけ書くと不思議なことのように思えますが、原因はおそらく単純です。細胞の培養液には牛の血清が添加されており、その中に含まれていたC1qがコンタミしたと考えられます。低温電子顕微鏡を使った構造解析では、形が似ているタンパク質粒子をグループとしてまとめて分けていくので、これだけ形が特徴的なら、C1qの存在は我々の目的タンパク質の構造解析ではあまり問題にはならない可能性が高いです。今回の日記のネタにもなってくれて、これまで出くわした多数のコンタミの中で、一番良いコンタミといえるかもしれません。
引用1
Hungler, A., Momin, A., Diederichs, K. & Arold, S., T. ContaMiner and ContaBase: a webserver and database for early identification of unwantedly crystallized protein contaminants. J. Appl. Crystallogr. 49, 2252–2258 (2016). https://pmc.ncbi.nlm.nih.gov/articles/PMC5140001/
引用2
Antonysamy, S. et al. Crystal structure of the human PRMT5:MEP50 complex. Proc. Natl. Acad. Sci. 109, 17960–17965 (2012). https://pubmed.ncbi.nlm.nih.gov/23071334/
引用3
Bally, I. et al. Expression of recombinant human complement C1q allows identification of the C1r/C1s-binding sites. Proc. Natl. Acad. Sci. 110, 8650–8655 (2013). https://pmc.ncbi.nlm.nih.gov/articles/PMC3666734/
![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)


津山 泰一 (奨励研究員)
所属: 細胞・発生・進化研究室