VOL.2 細胞系譜の再検討
近藤寿人(JT生命誌研究館 顧問・表現ディレクター)
今回は、受精卵あるいは少し発生が進んだ段階の胚の中の、体細胞(骨や、神経や、血球など)になるずっと前の段階(「多分化能」をもつと表現されることが多い)の細胞たちから、いろいろな体細胞が生まれてくるまでの過程を見ることにしましょう。細胞が分裂して数を増やしつつ、それまで(親細胞)と異なった(娘)細胞を生み出してゆく過程の積み重ね(発生の経路)は、「細胞系譜」とも呼ばれます。
この細胞系譜を俯瞰する上で、教科書などにも取り上げられることから支配的な通説になっていた「三胚葉説」や「エピジェネティック・ランドスケープ epigenetic landscape」について検討してゆきます。結論を先に言えば、三胚葉説は全く実験的な根拠をもたないモデルです。一方、エピジェネティック・ランドスケープは、私が敬愛するConrad H. Waddington (コンラッド・ウォディントン) が1950年代半ば——DNAが遺伝物質の実体であることが示されてからまもない頃——に、その優れた発想から描いた比喩(metaphor)が、その真意をねじ曲げられたうえで現在引用されているという、残念な状況です。
科学は、それまでの通説と矛盾する現象に出会った時に、それを「例外」と見なすのではなく、その現象を矛盾なく説明する新しいモデル(理解の枠組み)を組み立てることによって進歩します。例えば、天体の中で、「惑星」と呼ばれる一群の星が、東から上ったと思えば、ブーメランのように東に沈むなど「恒星」とは異なった不規則な動きをするのを見て、「惑星は、地球の周りでそのような不規則なうごきをする星である」と言って満足する人は天動説に留まり、一方、「地球は惑星の一つであって、太陽の周りを自転しながら廻っているのだ」という美しい全体像を描けた科学者が、正しい地動説にたどり着きました。発生生物学も、地動説に相当する、新しい全体像を構築する時期に来ています。
三胚葉説
三胚葉説は、「細胞系譜は、まず外胚葉、中胚葉、内胚葉という、大きな3つの系譜に分かれ、胚葉ごとにさらに系譜が細かく分岐してゆく。神経系は外胚葉が分かれてから外胚葉から発生するので、中胚葉に分岐してから起きる筋肉や骨の発生とは、細胞系譜上の繋がりはない」といったモデルです(図1A)。
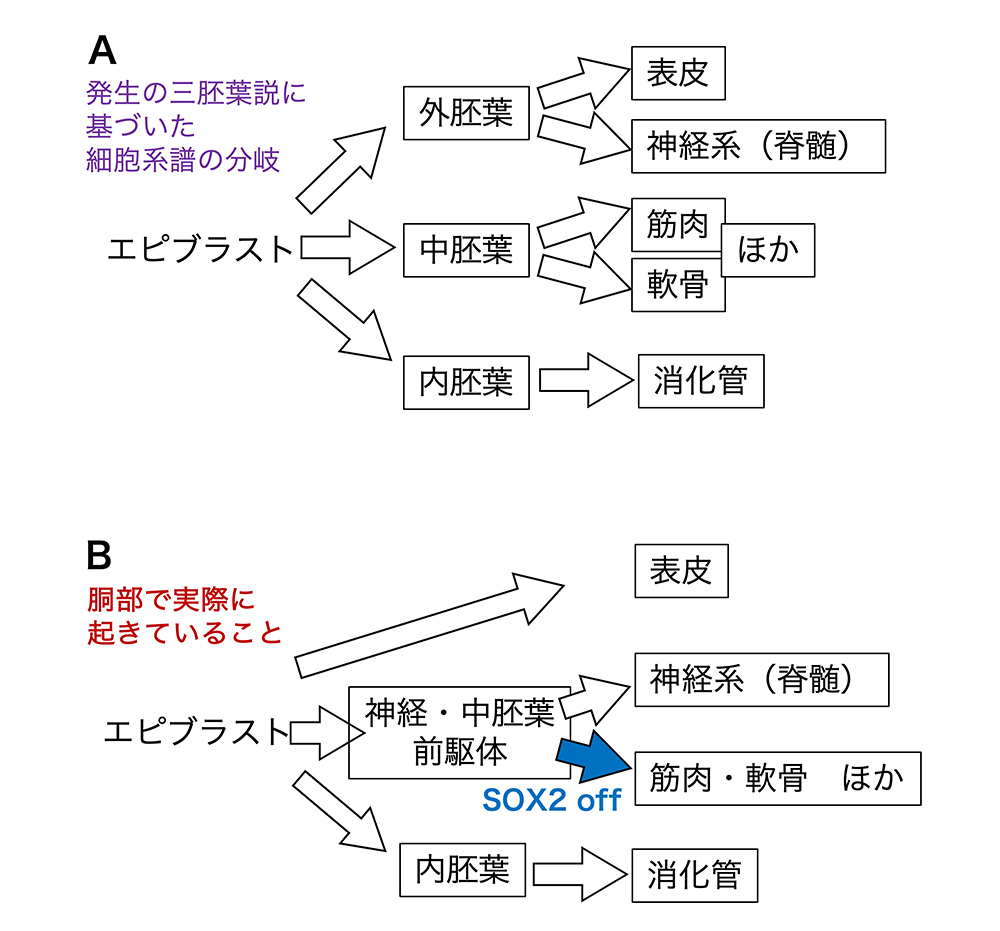
(図1)発生の三胚葉説が唱える細胞系譜は、実際には起きない
三胚葉は、もともとは解剖学上の表現で、胚の時期に体の表面を覆う細胞層を「外胚葉」、消化管の内腔をつくる細胞層を「内胚葉」、その間に挟まれる多種多様の組織を中胚葉と呼びます。その解剖学的な記載を、いつ誰が発生のプロセスと結びつけたのかは不明です。私自身、1960年以前の大家たちの著作を漁ってみましたが、発生の三胚葉説を述べている者は誰一人としていません。ある時にある病理学者が教科書に「発生の三胚葉説」を書いたのが流布してしまったらしいということを耳にしたのみです。いずれにせよ、「発生の三胚葉説」は、実験による裏付けをもたない状態で、天動説のように流布してしまったのです。前置きが長くなりました。本論に入りましょう。
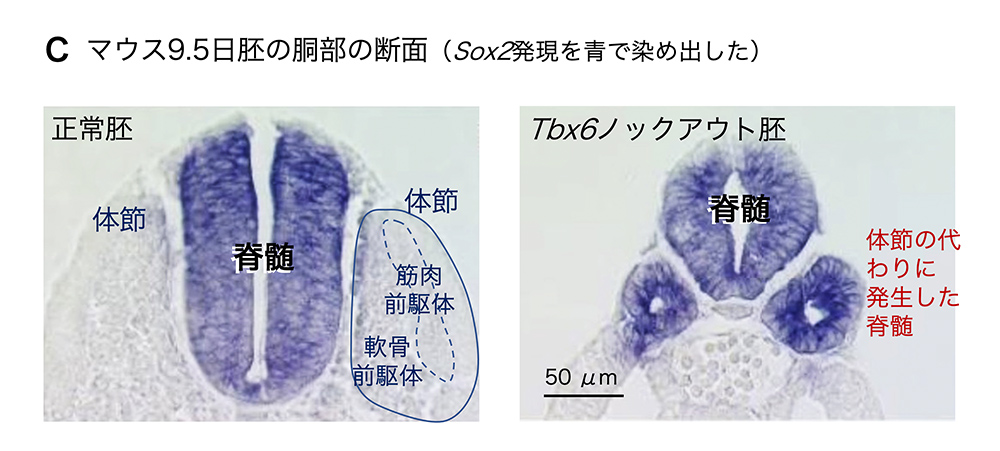
「Tbx6ノックアウトマウス胚では、筋肉や骨(軟骨)の前駆体である体節の代わりに、一対の余分な脊髄ができる(図1C)。」この驚くべき現象を報告するVirginia E. Papaioannou (ヴァージニア・パパイオアヌウ)のグループの論文が、1998年のNature誌に掲載されました[1]。これは「発生の三胚葉説」の破綻を示すものだと私は確信したのですが、なぜこのような現象が起きるのかを解析する研究はその後ありませんでした。
私たちは、神経系の発生の初期に中心的な役割を果たす転写因子SOX2のはたらきとその元になる遺伝子Sox2の発現について、主にニワトリ胚を用いて研究していました。胚の表面に位置する細胞(位置的には外胚葉)は、最初は前回お話しした「エピブラスト――全ての体細胞のもと」で占められています。エピブラストから出発して、「原腸陥入」と総称される細胞移動によって、内胚葉や、多種多様の中胚葉組織が生まれます。エピブラストの左右の中央を占める領域は、次に神経系のもとである神経板をつくる準備として、転写因子SOX2を弱く発現するようになるのですが、その準備を済ませたはずの細胞の一部が原腸陥入によって直下の中胚葉の層に移動すると、そのSOX2の発現を止めて、体節をつくることに気づきました[2]。つまり、(少なくともある発生ステージでは)神経板の前駆体は同時に体節の前駆体でもあるのです。現在では、多くの脊椎動物種でこのことは確認されていて、神経・中胚葉前駆体(NMP, neuromesodermal progenitor)と呼ぶのが一般的になっています(といっても、中胚葉に位置する組織のうちで、体節をつくるだけなのですが)。
もしその神経・中胚葉前駆体が中胚葉の区画に移動した際に、SOX2の発現を止めることができなかったら、体節ができるはずの場所で胴体の神経系(脊髄)をつくるに違いない。Tbx6のノックアウトマウス胚で起きていることはまさにこのことであるに違いないと、2006年の論文[2]で述べたのですが、まだ仮説の段階だったのであまり注目されませんでした。その後、PapaioannouさんからTbx6ノックアウトマウス(ヘテロ接合体では発生は正常)を送ってもらって、その胚を調べたところ、Tbx6ノックアウトマウス胚では、体節の場所に移動した神経・中胚葉前駆体がSOX2を発現し続けることを確認しただけでなく、正常胚の中でも、体節の前駆体でSOX2を強制発現すれば体節が脊髄に発生することも示しました[3]。2011年のことです。
以上の研究は、胚組織の系譜はまず三胚葉に分かれるという「発生の三胚葉説」が成り立たないことを示しました(図1B)。さらに、原腸陥入は、遺伝子発現の変化を起こす契機に過ぎず、細胞移動自体が発生運命(系譜)を支配するわけではないことも示しました。「発生の三胚葉説」に対する強い反例は、今回の最後の方でもとりあげます。
私たちの結論は、高校の生物学の教科書の一つが取り上げてくれました。NMPが発生生物学の常識(少なくともプロの間では)となった今、高校の教科書で「発生の三胚葉説」を積極的に取り上げるのは見直していただきたいと思っています。
エピジェネティック・ランドスケープ
C. H. Waddingtonは、1950年頃にはすでに、胚発生のプロセスは遺伝子のはたらきの切り換わりの連鎖で進行すると考えていました。当時すでに、ショウジョウバエの形態に反映されるさまざまな変異体が見つかっており、それらの変異体からイマジネーションをかき立てられて到達した論考であったのでしょう。発生過程は遺伝子(gene)の作用の連鎖の結果もたらされる(epi)ものであることから、彼は発生過程のことをepigeneticsと呼びました。現代のepigenetics(ATGCで表される塩基配列の枠を超えた調節機構)とは意味合いが違います。彼が1952年に著した“The epigenetics of birds”は、鳥類の発生に題材を求めた、発生の調節に関する研究書です。
彼は、遺伝子の作用の連鎖の分岐で分かれてゆく細胞系譜のイメージを描画の比喩で表現することを思い立ち、それをエピジェネティック・ランドスケープ(epigenetic landscape)と呼びました[4][5]。訳せば「発生の進行を風景画で擬える」といったところでしょうか。エピジェネティック・ランドスケープを描いた目的には、細胞系譜の分岐を読者にイメージさせることとともに、遺伝子のはたらきの変化(例えばショウジョウバエの変異体で見られるような)によって、発生過程がどのように変化しうるかということもイメージさせようという、優れた意図があったのです。図2では、Waddingtonの作図に模して、この2つのポイントを表現してみました。
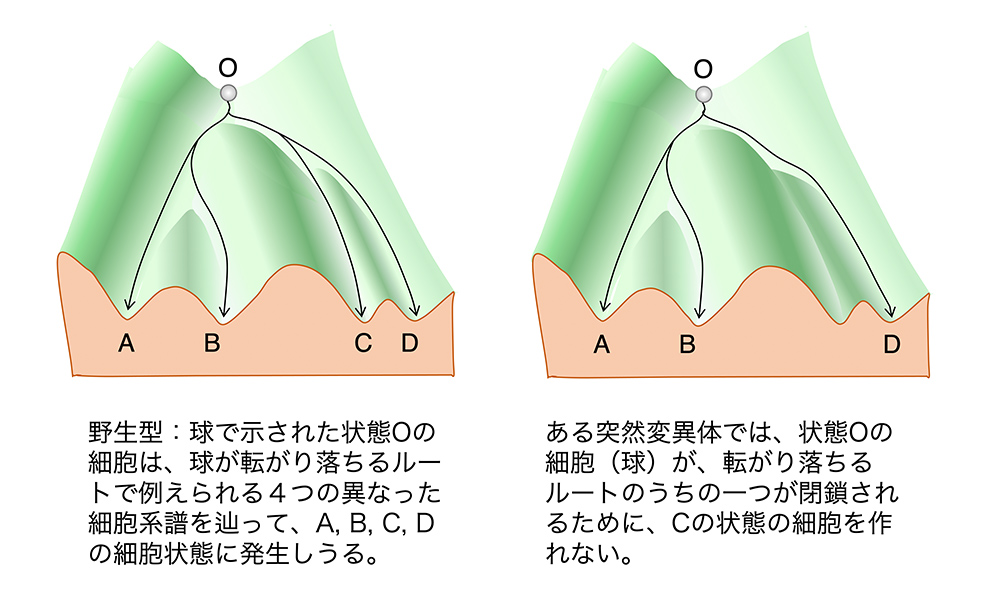
(図2)エピジェネティック・ランドスケープを用いた、細胞系譜の分岐と、突然変異による効果についての比喩表現
しかし、エピジェネティック・ランドスケープの「細胞系譜の分岐をイメージさせる」効果は強烈で、この面だけが一人歩きを始めました。また、古典期のそして誤った発生観である「細胞分化は逆行しない」であるとか、「特定の体細胞を生み出すには、特定の細胞系譜を辿らなければならない」といった見方(いずれにもWaddingtonは関わっていない)にも合致したために、エピジェネティック・ランドスケープが、神格化された教義のようにみなされる由々しき状況が起きてしまいました。前回に述べた「オーガナイザー」の神格化に似た点があります。現在では、以下に述べる実例、さらにはiPS細胞などの研究によって、発生のプロセスが、エピジェネティック・ランドスケープの比喩ではとても収まりきらない自在性をもっていることが明らかになっています。
この現在においてなお、エピジェネティック・ランドスケープの坂をボールが遡るような作図や、ある点から別の点にワープするような軌跡をエピジェネティック・ランドスケープの上に描くような作図が氾濫しています。新しい発見を、旧来の考え方の枠組みに埋め込めばどうなるかという表現としてはうなずけるのですが、そろそろ発生生物学はエピジェネティック・ランドスケープの世界観から脱皮する時期に達していると思います。以下の節で、エピジェネティック・ランドスケープの世界観からの脱皮を促す、代表的な例を紹介しましょう。
水晶体を生み出す異なった細胞系譜が、いくつもある
私は、前回そして今回の第1節で述べた、神経系発生の初期段階を研究する前には、水晶体を具体例として、特定の体細胞組織を成立させる機構について研究していました。そして、2つの転写因子SOX2とPAX6が同時に作用する条件が実現されると、細胞は水晶体発生の準備状態になり[6]、それにさらにPROX1という第3の転写因子が加わると、透き通って球形の水晶体組織(中には、クリスタリンと総称される水晶体固有のタンパク質が詰まっている)が発生することがわかりました。この2段階の水晶体発生は、頭部の表皮が網膜の前駆体と相互作用して始まる通常の目の水晶体の発生でも、イモリで起きる、目の虹彩を出発点とした水晶体再生でも確認されます。(詳しくは、動画「再生力のチャンピオン イモリとプラナリアのワザ比べ」10分24秒から14分28秒をご覧ください)
しかし、「2つの転写因子SOX2とPAX6を同時に発現する」組織は、他にもあるのです。一つの例は、目の網膜、もう一つの例は、下垂体前葉(さまざまなホルモンを分泌する)の前駆体です。これらの組織は、果たして、水晶体発生の準備状態にあるのでしょうか?答えはYESでした。私たちは、これらの組織が水晶体発生の準備状態にあったとしても、次の段階のPROX1の発現が何らかの機構で抑えられているために、水晶体の発生には進まないのだろうと予測し、次の実験を行いました。
<網膜の場合>
孵卵8日のニワトリ胚の眼の中では、網膜の多種類のニューロンやグリア(ミュラー細胞と呼ばれます)が分化を遂げています。そのニワトリ胚網膜の細胞を培養皿の上に培養すると、胚の網膜の細胞組成を反映して、ミュラー細胞の上にニューロンの細胞が集塊をつくります。SOX2とPAX6の発現は続いています。その状態では、細胞間の接触に依存したNotch(ノッチ)シグナルが細胞の状態を安定化していることが予想されたので、ノッチシグナルの阻害剤を培養に加えてみました。すると、2日後にはPROX1の発現が急上昇し、2週間後には、それまでニューロンであった細胞もグリアであった細胞も、ほとんどが水晶体の細胞になってしまいました。このことから、SOX2とPAX6を発現する網膜の細胞には、水晶体に分化する潜在能力があること、そしてその潜在能力はノッチシグナルによって抑えられていることが明らかになりました(図3A)[7]。
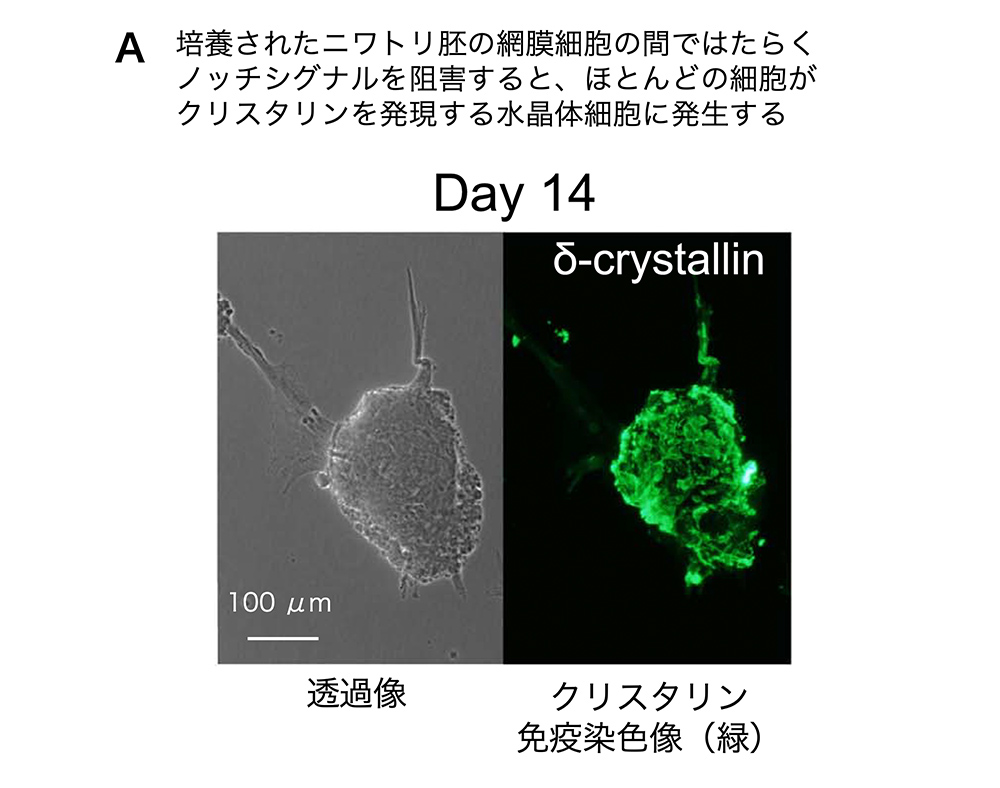
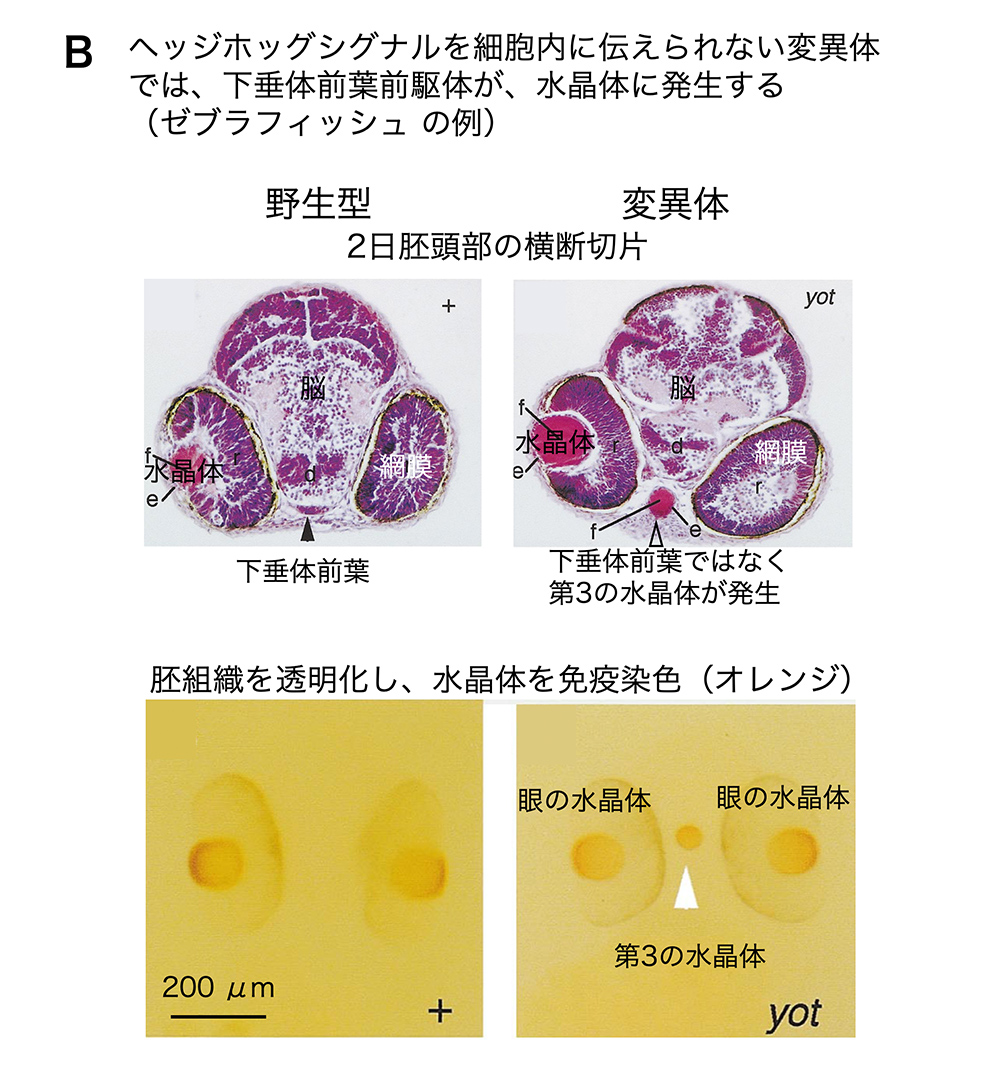
(図3)SOX2とPAX6を発現する胚組織から、水晶体が発生する
<下垂体前葉の前駆体の場合>
もう一つの例は、下垂体前葉の前駆体です。下垂体前葉の前駆体が正常に発生するには、Hedgehog(ヘッジホッグ)シグナルがはたらかなければなりません。現在広島大学教授である都築政起氏が若い日に見つけられた変異体(HMM, ここではTalpidと呼びます)の胚ではヘッジホッグシグナルがはたらいていないことが明らかになったので、その受精卵を名古屋大学の鳥類バイオサイエンス研究センター(ナショナルバイオリソース「ニワトリ・ウズラ」の拠点)から提供して頂きました。Talpid変異ウズラ胚の下垂体前葉前駆体の発生を調べたところ(下垂体前葉前駆体が複数出現するという予想外のこともあったのですが)それらの前駆体の中に、SOX2, PAX6, PROX1, クリスタリンを発現する立派な水晶体ができることがわかりました[8]。下垂体前葉の前駆体にヘッジホッグシグナルが作用しなければその一部が水晶体に発生することは、小型魚ゼブラフィッシュでも確認されていますので(図3B)[9]、広い範囲の脊椎動物に当てはまると考えられます。
<転写因子の作用が重要>
これらの研究の結果は、次のことを示しています。「特定の体細胞を生み出すには、特定の細胞系譜を辿らなければならない」ことは決してありません。特定の体細胞を生み出すのは、その体細胞を生み出すのに必要な一群の転写因子が、特定の順序で作用するかどうかにかかっているのです。
心臓に発生するはずだった心臓の前駆体が、急遽、脳に発生してしまう場合
今回の最後に、細胞系譜の意味について深く再考せざるを得ない現象についてお話ししましょう。Benoit G. Breuneau (ブノワ・ブルノー)は、マウスのES細胞から出発した細胞集団を、ほとんど100%の効率で心筋細胞に発生させる培養操作技術(細胞を塊にして培養したり、単層で培養したり、VEGFを主体としたさまざまな因子を加えたり除いたりする)を確立し、それを用いて心筋の発生に関わる制御に関する研究を展開してきました。ところが、ES細胞としてBrmという遺伝子を欠損した細胞を用いると、心筋の前駆体細胞は正常にできるのに(培養4日目)、その心筋に発生するはずの細胞が急遽(培養6日には)、脳の神経前駆細胞に発生してしまって、心筋細胞が全くできなくなったのです(図4)[10]。Brm遺伝子がつくるBRMは、転写因子をゲノムの中の特定の領域に結合させるかどうかという制御に関わるタンパク質の一つですが、それがなくなったことの(おそらく間接的な)効果として、心筋を前駆体から発生させるための転写因子が起動せず、一方で、SOX2, OCT6, OTX2といった脳の神経を発生させる転写因子が起動されていました。先に述べた、『特定の体細胞を生み出すのは、その体細胞を生み出すのに必要な一群の転写因子が、特定の順序で作用するかどうかにかかっている』ことを裏付けるものです。
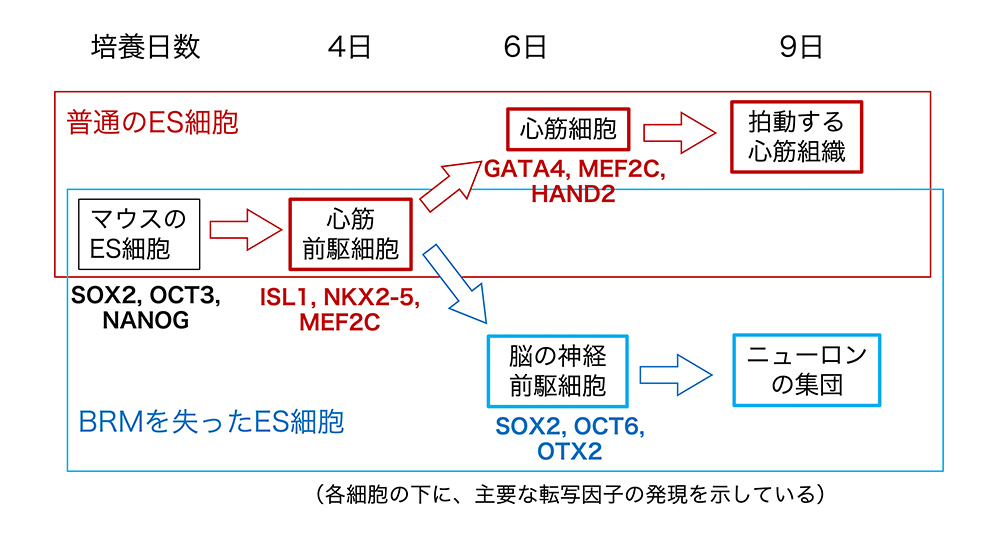
(図4)心筋に発生するはずの心筋前駆細胞が、急遽、脳の神経前駆細胞に変化してしまう場合
しかし、この結果はマウスのES細胞から出発した発生に関するものでした。マウスの中でも同じことは起きるのでしょうか?Brm遺伝子と、その兄弟遺伝子Brg1を同時に心臓の前駆体で失わせたマウス胚では、心筋は発生しませんーーここまではES細胞から出発した場合に似ていますが、心筋の代わりに脳が発生するわけではありませんでした[10]。ES細胞から出発した発生が「不完全」だからでしょうか?そうではありません。ES細胞から出発した発生の経路(細胞系譜)は、胚の中でみられる発生の経路とよく似ていることもあるし、かなり違っていることもあるのです。初期胚の状態から特定の体細胞に辿り着く経路には、かなりのヴァリエーションあるいは選択肢があって(前節はその一例)、その中のほぼ一つの経路だけが胚発生で採用されている(潜在する他の経路は抑制される)と考えるのが妥当でしょう。胚発生では、いろいろな組織をつくり出すだけでなく、異なった組織の組み合わせで機能をもった器官をつくり上げ、また、器官同士を機能・構造の両面で連携しなければなりません。そのために、ある特定のタイミングで、また胚の中の特定の位置で、特定の組織のセットを生み出さなければならない。この条件を満たすように転写因子の活性化が時間的・空間的に制御され(その制御に、細胞間のシグナル機構がはたらいて、細胞群の動機的な変化をも保証する)、その結果としてもたらされるのが、胚発生の過程で観察される細胞系譜なのです。
引用文献
[1] Chapman DL, Papaioannou VE. Three neural tubes in mouse embryos with mutations in the T-box gene Tbx6. Nature. 1998 391(6668):695-7. doi: 10.1038/35624.
[2] Takemoto T, Uchikawa M, Kamachi Y, Kondoh H. Convergence of Wnt and FGF signals in the genesis of posterior neural plate through activation of the Sox2 enhancer N-1. Development. 2006 133(2):297-306. doi: 10.1242/dev.02196.
[3] Takemoto T, Uchikawa M, Yoshida M, Bell DM, Lovell-Badge R, Papaioannou VE, Kondoh H. Tbx6-dependent Sox2 regulation determines neural or mesodermal fate in axial stem cells. Nature. 2011 470(7334):394-8. doi: 10.1038/nature09729.
[4] Waddington CH. Principles of embryology. 1956. George Allen & Unwin.
[5] Waddington CH. The strategy of the genes. 1957. George Allen & Unwin.
[6] Kamachi Y, Uchikawa M, Tanouchi A, Sekido R, Kondoh H. Pax6 and SOX2 form a co-DNA-binding partner complex that regulates initiation of lens development. Genes Dev. 2001 15(10):1272-86. doi: 10.1101/gad.887101.
[7] Iida H, Ishii Y, Kondoh H. Intrinsic lens potential of neural retina inhibited by Notch signaling as the cause of lens transdifferentiation. Dev Biol. 2017 421(2):118-125. doi: 10.1016/j.ydbio.2016.11.004.
[8] Taira Y, Ikuta Y, Inamori S, Nunome M, Nakano M, Suzuki T, Matsuda Y, Tsudzuki M, Teramoto M, Iida H, Kondoh H. The formation of multiple pituitary pouches from the oral ectoderm causes ectopic lens development in hedgehog signaling-defective avian embryos. Dev Dyn. 2020 49(12):1425-1439. doi: 10.1002/dvdy.222.
[9] Kondoh H, Uchikawa M, Yoda H, Takeda H, Furutani-Seiki M, Karlstrom RO. Zebrafish mutations in Gli-mediated hedgehog signaling lead to lens transdifferentiation from the adenohypophysis anlage. Mech Dev. 2000 96(2):165-74. doi: 10.1016/s0925-4773(00)00387-7.
[10] Hota SK, Rao KS, Blair AP, Khalilimeybodi A, Hu KM, Thomas R, So K, Kameswaran V, Xu J, Polacco BJ, Desai RV, Chatterjee N, Hsu A, Muncie JM, Blotnick AM, Winchester SAB, Weinberger LS, Hüttenhain R, Kathiriya IS, Krogan NJ, Saucerman JJ, Bruneau BG. Brahma safeguards canalization of cardiac mesoderm differentiation. Nature. 2022 602(7895):129-134. doi: 10.1038/s41586-021-04336-y.
図の引用
サムネイル及び図1C. 文献3 Fig. 3(SPRINGER NATUREから転載許可)
図3A. 文献7 Fig. 1(ELSEVIERから転載許可)
図3B. 文献9 Fig. 1(ELSEVIERから転載許可)
バックナンバー
VOL.4 胚のいつ、どこで、何を発生させるのかには欠かせない抑制機構
VOL.8 動物の形の多様性という名の変奏曲集I 目と顔と手
![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)

